Haydari MN, Perron MC, Laprise S, Roy O, Cameron JD, Proulx S, Brunette I. A short-term in vivo experimental model for Fuchs endothelial corneal dystrophy. Invest Ophthalmol Vis Sci. 2012 Sep 19;53(10):6343-54.
Impact scientifique: La dystrophie de Fuchs est une maladie dégénérative de l’œil, où la cornée se gonfle d’eau et perd sa transparence. Ceci résulte en des éblouissements et une perte de vision douloureuse. La greffe de cornée est traditionnellement le seul traitement pour cette maladie qui est responsable à elle seule de plus du quart des 50 000 greffes de cornée effectuées chaque année au Canada et aux USA. Or, les banques d’yeux ne suffisent plus à la demande sans cesse croissante et de nouvelles sources de tissu sain sont nécessaires. Ce papier démontre, pour la première fois, qu’il est possible de cultiver, sans manipulation génétique, les cellules cornéennes endothéliales de patients atteints de dystrophie de Fuchs. Ces cellules ont été utilisées pour développer des modèles in vitro et in vivo uniques permettant d’étudier cette maladie. Ces cellules ont aussi permis de reconstruire un endothélium cornéen fonctionnel une fois transplanté chez l’animal. Ces résultats ouvrent la porte vers une toute nouvelle avenue thérapeutique, où un patient pourrait être traité avec ses propres cellules.
Contribution du Réseau: Le RRSV a fourni les cellules endothéliales des cornées humaines normales et atteintes d’une dystrophie de Fuchs (Banque de tissus oculaires) nécessaires à ce projet multidisciplinaire en collaboration avec plusieurs équipes.
* * *
Résumé Original
Purpose: We evaluated the in vivo functionality of a corneal endothelium tissue-engineered using corneal endothelial cells from human patients with Fuchs endothelial corneal dystrophy (FECD). Methods: A total of 15 healthy cats underwent full-thickness corneal transplantation. All transplants were of xenogeneic human origin and all grafts but two were tissue-engineered. In seven animals the graft corneal endothelium was tissue-engineered using cultured corneal endothelial cells from humans with FECD (TE-FECD). Two control animals were grafted with an endothelium engineered using cultured endothelial cells from normal eye bank corneas (TE-normal). Two controls received a native full-thickness corneal transplant, and four other controls were grafted with the stromal carrier only (without endothelial cells). Outcome parameters included graft transparency (0, opaque to 4, clear), pachymetry, optical coherence tomography, endothelial cell morphometry, transmission electron microscopy (TEM), and immunostaining of function-related proteins. Results: Seven days after transplantation, 6 of 7 TE-FECD grafts, all TE-normal grafts, and all normal native grafts were clear (transparency score >3), while all carriers-only grafts were opaque (score <1). The mean pachymetry was 772 ± 102 μm for TE-FECD, 524 ± 11 μm for TE-normal, 555 ± 48 for normal native, and 1188 ± 223 μm for carriers only. TEM showed subendothelial loose fibrillar material deposition in all TE-FECD grafts. The TE endothelium expressed Na(+)-K(+)/ATPase and Na(+)/HCO3(-). Conclusions: Restoration of transparency and corneal thickness demonstrated that the TE-FECD grafts were functional in vivo. This novel FECD seven-day living model suggests a potential role for tissue engineering leading to FECD cell rehabilitation.
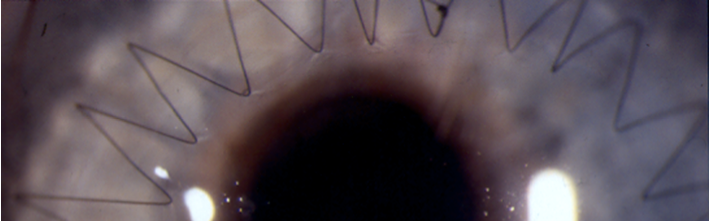
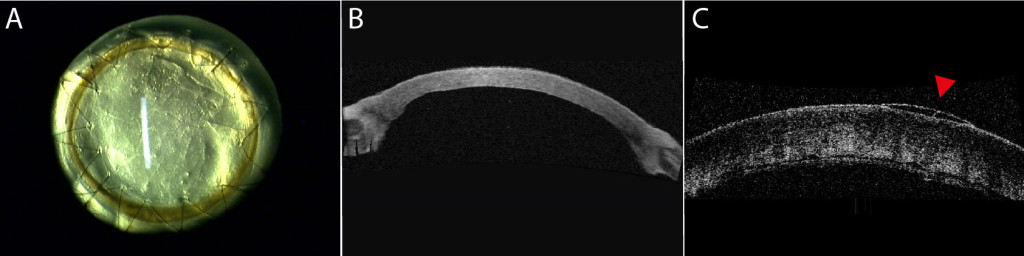
Modèle expérimental in-vivo de dystrophie de Fuchs (A, B) et son contrôle oedmacié, sans endothlium (C).